Нейродегенеративті аурулар(NDD) ми немесе жұлын ішіндегі белгілі бір осал нейрондық популяциялардың үдемелі немесе тұрақты жоғалуымен сипатталады. NDD жіктелуі әртүрлі критерийлерге негізделуі мүмкін, соның ішінде нейродегенерацияның анатомиялық таралуы (мысалы, экстрапирамидтік бұзылулар, фронтотемпоральды дегенерация немесе жұлын-ми миының атаксиялары), бастапқы молекулалық ауытқулар (мысалы, амилоид-β, приондар, тау немесе α-синуклеин) немесе негізгі клиникалық белгілер (мысалы, Паркинсон ауруы, амиотрофиялық бүйірлік склероз және деменция). Жіктелу мен симптомдардың көрінісіндегі осы айырмашылықтарға қарамастан, Паркинсон ауруы (PD), амиотрофиялық бүйірлік склероз (ALS) және Альцгеймер ауруы (AD) сияқты бұзылулар нейрондық дисфункцияға және ақырында жасуша өліміне әкелетін ортақ негізгі процестерге ие.
Дүниежүзілік денсаулық сақтау ұйымының бағалауы бойынша, әлемде миллиондаған адам NDD-ден зардап шегеді, сондықтан 2040 жылға қарай бұл аурулар дамыған елдерде өлімнің екінші басты себебіне айналады. Белгілі бір аурулармен байланысты симптомдарды жеңілдету және басқару үшін әртүрлі емдеу әдістері қолжетімді болғанымен, бұл жағдайлардың дамуын баяулатудың немесе емдеудің тиімді әдістері әлі күнге дейін белгісіз. Жақында жүргізілген зерттеулер емдеу парадигмаларының жай ғана симптомдық басқарудан одан әрі нашарлаудың алдын алу үшін жасушаларды қорғау механизмдерін пайдалануға ауысқанын көрсетеді. Кең ауқымды дәлелдер тотығу стрессі мен қабынудың нейродегенерацияда маңызды рөл атқаратынын және бұл механизмдерді жасушаларды қорғаудың маңызды нысаналары ретінде көрсететінін көрсетеді. Соңғы жылдары іргелі және клиникалық зерттеулер нейродегенеративті ауруларды емдеудегі гипербариялық оттегі терапиясының (ГОТ) әлеуетін ашты.
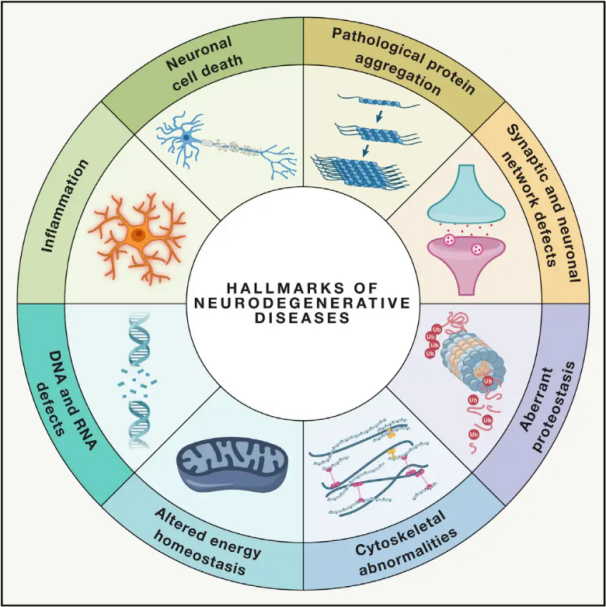
Гипербариялық оттегі терапиясын (ГОТ) түсіну
HBOT әдетте 1 абсолютті атмосферадан (ATA) жоғары қысымды - теңіз деңгейіндегі қысымды - 90-120 минутқа дейін арттыруды қамтиды, көбінесе емделіп жатқан нақты жағдайға байланысты бірнеше сеансты қажет етеді. Ауа қысымының жоғарылауы жасушаларға оттегінің жеткізілуін жақсартады, бұл өз кезегінде бағаналы жасушалардың көбеюін ынталандырады және белгілі бір өсу факторлары арқылы емделу процестерін күшейтеді.
Бастапқыда HBOT қолдануы Бойль-Мариотт заңына негізделген, ол газ көпіршіктерінің қысымға тәуелді азаюын және тіндердегі оттегінің жоғары деңгейінің пайдасын көрсетеді. HBOT тудыратын гипероксикалық күйден пайда көретін бірқатар патологиялар белгілі, соның ішінде некротикалық тіндер, радиациялық жарақаттар, жарақат, күйіктер, компартмент синдромы және газ гангренасы, Су асты және гипербариялық медициналық қоғам тізімдеген басқалары бар. Атап айтқанда, HBOT колит және сепсис сияқты әртүрлі қабыну немесе жұқпалы аурулар модельдерінде қосымша емдеу ретінде де тиімділігін көрсетті. Қабынуға қарсы және тотығу механизмдерін ескере отырып, HBOT нейродегенеративті ауруларды емдеудің терапиялық жолы ретінде айтарлықтай әлеуетке ие.
Нейродегенеративті аурулардағы гипербариялық оттегі терапиясының клиникаға дейінгі зерттеулері: 3×Tg тышқан моделінен алынған түсініктер
Белгілі зерттеулердің біріАльцгеймер ауруының (АА) 3×Tg тышқан моделіне назар аударылды, ол HBOT-тың когнитивтік кемшіліктерді жақсартудағы терапиялық әлеуетін көрсетті. Зерттеуге 17 айлық еркек 3×Tg тышқандары қатысты, ал бақылау тобында қызмет ететін 14 айлық еркек C57BL/6 тышқандары қатысты. Зерттеу HBOT когнитивтік функцияны жақсартып қана қоймай, сонымен қатар қабынуды, бляшка жүктемесін және АА патологиясымен байланысты маңызды процесс - Тау фосфорлануын айтарлықтай төмендеткенін көрсетті.
HBOT қорғаныс әсерлері нейроқабынудың төмендеуімен байланысты болды. Бұл микроглия пролиферациясының, астроглиоздың және қабынуға қарсы цитокиндердің секрециясының төмендеуімен дәлелденді. Бұл зерттеулер HBOT-тың Альцгеймер ауруымен байланысты нейроқабыну процестерін бір уақытта азайта отырып, когнитивті өнімділікті арттырудағы қос рөлін атап көрсетеді.
Тағы бір клиникаға дейінгі модель HBOT-тың нейрондық функция мен қозғалыс мүмкіндіктеріне қорғаныс механизмдерін бағалау үшін 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (MPTP) тышқандарын пайдаланды. Нәтижелер HBOT бұл тышқандарда қозғалыс белсенділігі мен ұстау күшін арттыруға ықпал еткенін, митохондриялық биогенез сигнализациясының артуымен, атап айтқанда SIRT-1, PGC-1α және TFAM белсендірілуі арқылы өзара байланысты екенін көрсетті. Бұл HBOT-тың нейропротекторлық әсерлеріндегі митохондриялық функцияның маңызды рөлін көрсетеді.
Нейродегенеративті аурулардағы HBOT механизмдері
NDD үшін HBOT қолданудың негізгі қағидасы оттегінің азаюы мен нейродегенеративті өзгерістерге сезімталдық арасындағы байланыста жатыр. Гипоксия-индукцияланатын фактор-1 (HIF-1) жасушалардың төмен оттегі кернеуіне бейімделуін қамтамасыз ететін транскрипция факторы ретінде орталық рөл атқарады және AD, PD, Хантингтон ауруы және ALS сияқты әртүрлі NDD-лерде кездеседі, бұл оны маңызды дәрілік нысана ретінде белгілейді.
Жасы көптеген нейродегенеративті бұзылулардың маңызды қауіп факторы болғандықтан, HBOT-тың қартаю нейробиологиясына әсерін зерттеу өте маңызды. Зерттеулер HBOT сау егде жастағы адамдарда жасқа байланысты когнитивтік кемшіліктерді жақсарта алатынын көрсетті.Сонымен қатар, есте сақтау қабілетінің айтарлықтай бұзылуы бар егде жастағы науқастар HBOT әсерінен кейін когнитивті жақсаруларды және ми қан ағымының жоғарылауын көрсетті.
1. HBOT-тың қабынуға және тотығу стрессіне әсері
HBOT мидың ауыр дисфункциясы бар науқастарда нейроқабынуды жеңілдету қабілетін көрсетті. Ол қабынуға қарсы цитокиндерді (IL-1β, IL-12, TNFα және IFNγ сияқты) төмендетумен қатар, қабынуға қарсы цитокиндерді (IL-10 сияқты) күшейту мүмкіндігіне ие. Кейбір зерттеушілер HBOT арқылы түзілетін реактивті оттегі түрлері (ROS) терапияның бірнеше пайдалы әсерін тудырады деп болжайды. Демек, оның қысымға тәуелді көпіршікті төмендету әсерінен және тіндердің оттегімен жоғары қанығуына қол жеткізуден басқа, HBOT-пен байланысты оң нәтижелер ішінара өндірілген ROS-тың физиологиялық рөлдеріне байланысты.
2. HBOT-тың апоптозға және нейропротекцияға әсері
Зерттеулер HBOT-тың p38 митогенмен белсендірілген ақуыз киназының (MAPK) гиппокампальды фосфорлануын төмендете алатынын, кейіннен когнитивті жақсартып, гиппокампальды зақымдануды азайта алатынын көрсетті. Жеке HBOT та, гинкго билоба сығындысымен бірге де Bax экспрессиясын және каспаза-9/3 белсенділігін төмендететіні анықталды, бұл aβ25-35 тудырған кеміргіштер модельдерінде апоптоз жылдамдығының төмендеуіне әкеледі. Сонымен қатар, тағы бір зерттеу HBOT-тың алдын ала шарттауы церебральды ишемияға төзімділікті тудыратынын, механизмдері SIRT1 экспрессиясының жоғарылауымен, В-жасушалық лимфома 2 (Bcl-2) деңгейінің жоғарылауымен және белсенді каспаза-3-тің төмендеуімен қатар HBOT-тың нейропротекторлық және апоптозға қарсы қасиеттерін атап көрсететінін көрсетті.
3. HBOT-тың қан айналымына әсері жәнеНейрогенез
HBOT әсеріне ұшыраған адамдар бассүйек-қан тамырлары жүйесіне көптеген әсерлермен байланысты болды, соның ішінде қан-ми тосқауылының өткізгіштігін арттыру, ангиогенезді ынталандыру және ісінуді азайту. Тіндерге оттегінің көбірек берілуін қамтамасыз етумен қатар, HBOTтамырлардың пайда болуына ықпал етедітамыр эндотелийінің өсу факторы сияқты транскрипция факторларын белсендіру және жүйке бағаналы жасушаларының көбеюін ынталандыру арқылы.
4. HBOT эпигенетикалық әсерлері
Зерттеулер адамның микротамырлық эндотелий жасушаларының (HMEC-1) гипербариялық оттегіге ұшырауы 8101 генді, соның ішінде жоғары және төмен экспрессияларды айтарлықтай реттейтінін көрсетті, бұл антиоксиданттық жауап жолдарымен байланысты ген экспрессиясының артуын көрсетеді.
Қорытынды
HBOT қолдану уақыт өте келе айтарлықтай жетістіктерге жетті, бұл оның клиникалық тәжірибеде қолжетімділігін, сенімділігін және қауіпсіздігін дәлелдеді. HBOT NDD үшін жапсырмадан тыс емдеу ретінде зерттеліп, кейбір зерттеулер жүргізілгенімен, бұл жағдайларды емдеуде HBOT тәжірибелерін стандарттау үшін мұқият зерттеулер жүргізу қажеттілігі әлі де өзекті болып қала береді. Оңтайлы емдеу жиілігін анықтау және пациенттер үшін пайдалы әсерлердің дәрежесін бағалау үшін қосымша зерттеулер жүргізу қажет.
Қысқаша айтқанда, гипербариялық оттегі мен нейродегенеративті аурулардың қиылысуы терапиялық мүмкіндіктерде перспективалы шекараны көрсетеді, бұл клиникалық жағдайларда зерттеуді және валидацияны жалғастыруды талап етеді.
Жарияланған уақыты: 2025 жылғы 16 мамыр

