Қазіргі заманғы медицина саласында антибиотиктер микробтық инфекциялармен байланысты аурушаңдық пен өлім-жітім деңгейін күрт төмендетіп, ең маңызды жетістіктердің бірі болып шықты. Олардың бактериялық инфекциялардың клиникалық нәтижелерін өзгерту қабілеті сансыз пациенттердің өмір сүру ұзақтығын ұзартты. Антибиотиктер хирургиялық араласулар, имплантациялар, трансплантациялар және химиотерапияны қоса алғанда, күрделі медициналық процедураларда өте маңызды. Дегенмен, антибиотиктерге төзімді патогендердің пайда болуы алаңдаушылық тудырып, уақыт өте келе бұл препараттардың тиімділігін төмендетіп келеді. Микробтық мутациялар пайда болған кезде антибиотиктердің барлық санаттарында антибиотиктерге төзімділік жағдайлары тіркелген. Микробқа қарсы препараттардың таңдау қысымы төзімді штамдардың көбеюіне ықпал етті, бұл жаһандық денсаулық сақтау үшін айтарлықтай қиындық тудырды.
Микробқа қарсы төзімділіктің өзекті мәселесімен күресу үшін антибиотиктерді қолдануды азайтумен қатар, төзімді патогендердің таралуын шектейтін тиімді инфекциялық бақылау саясатын енгізу қажет. Сонымен қатар, балама емдеу әдістеріне деген қажеттілік бар. Гипербариялық оттегі терапиясы (ГОТ) осы тұрғыда перспективалы әдіс ретінде пайда болды, ол белгілі бір уақыт ішінде белгілі бір қысым деңгейінде 100% оттегін ингаляциялауды қамтиды. Инфекцияларды емдеудің негізгі немесе қосымша әдісі ретінде HBOT антибиотикке төзімді патогендердің жедел инфекцияларын емдеуде жаңа үміт сыйлауы мүмкін.
Бұл терапия қабыну, көміртегі тотығымен улану, созылмалы жаралар, ишемиялық аурулар және инфекциялар сияқты әртүрлі жағдайларды емдеу үшін негізгі немесе балама емдеу ретінде жиі қолданылады. HBOT-тың инфекцияны емдеудегі клиникалық қолданылуы терең, бұл пациенттерге баға жетпес артықшылықтар береді.

Инфекциядағы гипербарикалық оттегі терапиясының клиникалық қолданылуы
Қазіргі дәлелдер HBOT-ты дербес және қосымша емдеу ретінде қолдануды сенімді түрде қолдайды, бұл жұқтырған науқастарға айтарлықтай пайда әкеледі. HBOT кезінде артериялық қандағы оттегі қысымы 2000 мм сын. бағ. дейін көтерілуі мүмкін, ал нәтижесінде пайда болатын жоғары оттегі-тін қысымы градиенті тіндердегі оттегі деңгейін 500 мм сын. бағ. дейін көтеруі мүмкін. Мұндай әсерлер ишемиялық ортада байқалатын қабыну реакциялары мен микроциркуляция бұзылыстарының жазылуын жеделдетуде, сондай-ақ компартмент синдромын басқаруда ерекше құнды.
HBOT иммундық жүйеге тәуелді жағдайларға да әсер етуі мүмкін. Зерттеулер HBOT аутоиммундық синдромдарды және антиген тудыратын иммундық реакцияларды басатынын, иммундық реакцияларды модуляциялау кезінде лимфоциттер мен лейкоциттердің айналымын азайту арқылы трансплантатқа төзімділікті сақтауға көмектесетінін көрсетеді. Сонымен қатар, HBOTемдеуді қолдайдысозылмалы тері зақымдануларында ангиогенезді ынталандыру арқылы, бұл қалпына келуді жақсартудың маңызды процесі. Бұл терапия сонымен қатар жараларды емдеудің маңызды кезеңі болып табылатын коллаген матрицасының түзілуін ынталандырады.
Белгілі бір инфекцияларға, әсіресе некроздаушы фасциит, остеомиелит, созылмалы жұмсақ тіндердің инфекциялары және инфекциялық эндокардит сияқты терең және емдеу қиын инфекцияларға ерекше назар аудару қажет. HBOT-тың ең көп таралған клиникалық қолданылуының бірі - көбінесе анаэробты немесе төзімді бактериялардан туындайтын тері-жұмсақ тіндердің инфекциялары мен оттегінің төмен деңгейімен байланысты остеомиелитке арналған.
1. Диабеттік аяқ инфекциялары
Диабеттік аяқДиабеттік аяқ инфекциялары (ДТЖ) қант диабетімен ауыратын науқастар арасында кең таралған асқыну болып табылады, бұл популяцияның 25%-ына дейін әсер етеді. Инфекциялар бұл жараларда жиі пайда болады (жағдайлардың 40%-80%-ын құрайды) және аурушаңдық пен өлімнің артуына әкеледі. Диабеттік табан инфекциялары (ДТЖ) әдетте әртүрлі анаэробты бактериялық патогендері анықталған полимикробты инфекциялардан тұрады. Фибробласт функциясының ақаулары, коллаген түзілуі мәселелері, жасушалық иммундық механизмдер және фагоцит функциясы сияқты әртүрлі факторлар қант диабетімен ауыратын науқастарда жаралардың жазылуына кедергі келтіруі мүмкін. Бірнеше зерттеулер терінің оттегімен қамтамасыз етілуінің бұзылуы ДТЖ-мен байланысты ампутацияның күшті қауіп факторы ретінде анықталды.
DFI емдеудің қазіргі нұсқаларының бірі ретінде, HBOT диабеттік аяқ жараларының жазылу жылдамдығын айтарлықтай арттыратыны, нәтижесінде ампутация мен күрделі хирургиялық араласулардың қажеттілігін азайтатыны туралы хабарланған. Бұл тек қана жабысқақ операциялар және тері трансплантациясы сияқты ресурстарды көп қажет ететін процедуралардың қажеттілігін азайтып қана қоймай, сонымен қатар хирургиялық нұсқалармен салыстырғанда төмен шығындар мен минималды жанама әсерлерді ұсынады. Чен және т.б. жүргізген зерттеу HBOT-тың 10-нан астам сеансы қант диабетімен ауыратын науқастарда жаралардың жазылу жылдамдығының 78,3%-ға жақсарғанын көрсетті.
2. Некроздаушы жұмсақ тіндердің инфекциялары
Некроздаушы жұмсақ тін инфекциялары (НТЖИ) көбінесе полимикробты болып табылады, әдетте аэробты және анаэробты бактериялық патогендердің тіркесімінен пайда болады және көбінесе газ түзілуімен байланысты. НТЖИ салыстырмалы түрде сирек кездесетінімен, олардың тез өршуіне байланысты өлім деңгейі жоғары. Уақытылы және тиісті диагностика және емдеу қолайлы нәтижелерге қол жеткізудің кілті болып табылады, және НТЖИ-ді басқарудың қосымша әдісі ретінде НТЖИ-де НТЖИ қолдану туралы даулар әлі де бар. Перспективалық бақыланатын зерттеулердің болмауына байланысты НТЖИ-де НТЖИ қолдану туралы даулар әлі де бар.Дәлелдер бұл NSTI науқастарында өмір сүру деңгейінің жақсаруымен және органдардың сақталуымен байланысты болуы мүмкін екенін көрсетеді.Ретроспективті зерттеу HBOT алатын NSTI науқастары арасында өлім-жітімнің айтарлықтай төмендегенін көрсетті.
1.3 Хирургиялық орыннан инфекциялар
SSI инфекцияның анатомиялық орнына байланысты жіктелуі мүмкін және аэробты және анаэробты бактерияларды қоса алғанда, әртүрлі патогендерден туындауы мүмкін. Стерилизация әдістері, профилактикалық антибиотиктерді қолдану және хирургиялық тәжірибедегі жақсартулар сияқты инфекцияны бақылау шараларындағы жетістіктерге қарамастан, SSI тұрақты асқыну болып қала береді.
Бір маңызды шолуда нейробұлшықет сколиозына жасалған хирургиялық араласуда HBOT-тың терең SSI-дің алдын алудағы тиімділігі зерттелген. Операция алдындағы HBOT SSI жиілігін айтарлықтай төмендетіп, жаралардың жазылуын жеңілдетуі мүмкін. Бұл инвазивті емес терапия жара тіндеріндегі оттегі деңгейі жоғарылайтын орта жасайды, бұл патогендерге қарсы тотығу-өлтіру әрекетімен байланысты. Сонымен қатар, ол SSI дамуына ықпал ететін қан мен оттегі деңгейінің төмендеуін шешеді. Басқа инфекцияны бақылау стратегияларынан басқа, HBOT әсіресе тоқ ішек процедуралары сияқты таза ластанған операциялар үшін ұсынылады.
1.4 Күйіктер
Күйіктер – бұл қатты ыстықтан, электр тогынан, химиялық заттардан немесе радиациядан туындаған жарақаттар және жоғары аурушаңдық пен өлім деңгейін тудыруы мүмкін. HBOT зақымдалған тіндердегі оттегі деңгейін арттыру арқылы күйіктерді емдеуде пайдалы. Жануарлар мен клиникалық зерттеулер аралас нәтижелер көрсеткенімен,күйікті емдеудегі HBOT тиімділігі, 125 күйік алған науқасты қамтитын зерттеу HBOT өлім-жітім деңгейіне немесе жасалған операциялар санына айтарлықтай әсер етпегенін, бірақ орташа жазылу уақытын қысқартқанын көрсетті (43,8 күнмен салыстырғанда 19,7 күн). HBOT-ны кешенді күйікпен емдеумен біріктіру күйік алған науқастарда сепсисті тиімді бақылауға мүмкіндік береді, бұл жазылу уақытын қысқартуға және сұйықтыққа деген қажеттілікті азайтуға әкеледі. Дегенмен, HBOT-тың кең көлемді күйіктерді емдеудегі рөлін растау үшін одан әрі кең ауқымды перспективалық зерттеулер қажет.
1.5 Остеомиелит
Остеомиелит – көбінесе бактериялық патогендерден туындайтын сүйек немесе сүйек кемігінің инфекциясы. Остеомиелитті емдеу сүйектерге қанның салыстырмалы түрде нашар жеткізілуіне және антибиотиктердің сүйек кемігіне шектеулі енуіне байланысты қиын болуы мүмкін. Созылмалы остеомиелит тұрақты патогендермен, жеңіл қабынумен және некрозды сүйек тінінің пайда болуымен сипатталады. Рефрактерлік остеомиелит тиісті емдеуге қарамастан жалғасатын немесе қайталанатын созылмалы сүйек инфекцияларын білдіреді.
HBOT жұқтырған сүйек тіндеріндегі оттегі деңгейін айтарлықтай жақсартатыны дәлелденген. Көптеген клиникалық жағдайлар сериясы мен когорттық зерттеулер HBOT остеомиелитпен ауыратын науқастардың клиникалық нәтижелерін жақсартатынын көрсетеді. Ол метаболикалық белсенділікті арттыру, бактериялық патогендерді басу, антибиотиктердің әсерін күшейту, қабынуды азайту және жазылуды жеделдету сияқты әртүрлі механизмдер арқылы жұмыс істейтін сияқты.процестер. HBOT-тан кейін созылмалы, рефрактерлік остеомиелитпен ауыратын науқастардың 60%-дан 85%-ға дейінінде инфекцияның басылу белгілері байқалады.
1.6 Саңырауқұлақ инфекциялары
Дүние жүзінде үш миллионнан астам адам созылмалы немесе инвазивті саңырауқұлақ инфекцияларынан зардап шегеді, бұл жыл сайын 600 000-нан астам адамның өліміне әкеледі. Саңырауқұлақ инфекцияларын емдеу нәтижелері көбінесе иммундық мәртебенің өзгеруі, негізгі аурулар және патогеннің вируленттілік сипаттамалары сияқты факторларға байланысты нашарлайды. HBOT қауіпсіздігі мен инвазивті емес сипатына байланысты ауыр саңырауқұлақ инфекцияларында тартымды терапиялық нұсқаға айналуда. Зерттеулер HBOT Aspergillus және Mycobacterium tuberculosis сияқты саңырауқұлақ патогендеріне қарсы тиімді болуы мүмкін екенін көрсетеді.
HBOT Aspergillus биофильмінің түзілуін тежеу арқылы зеңге қарсы әсерді күшейтеді, супероксиддисмутаза (SOD) гендерінің жетіспеушілігі бар штамдарда тиімділігінің артуы байқалады. Саңырауқұлақ инфекциялары кезіндегі гипоксиялық жағдайлар зеңге қарсы дәрілерді жеткізуде қиындықтар тудырады, бұл HBOT-тан оттегі деңгейінің жоғарылауын әлеуетті пайдалы араласу етеді, дегенмен әрі қарай зерттеулер жүргізу қажет.
HBOT-тың микробқа қарсы қасиеттері
HBOT жасаған гипероксидті орта бактерияға қарсы қасиеттерді ынталандыратын физиологиялық және биохимиялық өзгерістерді бастайды, бұл оны инфекцияға қарсы тиімді қосымша терапияға айналдырады. HBOT тікелей бактерицидтік белсенділік, иммундық реакцияларды күшейту және белгілі бір микробқа қарсы агенттермен синергетикалық әсер ету сияқты механизмдер арқылы аэробты бактерияларға және негізінен анаэробты бактерияларға қарсы керемет әсер көрсетеді.
2.1 HBOT-тың тікелей антибактериалды әсері
HBOT-тың тікелей бактерияға қарсы әсері негізінен жасушалық метаболизм кезінде пайда болатын супероксидті аниондар, сутегі асқын тотығы, гидроксил радикалдары және гидроксил иондары сияқты реактивті оттегі түрлерінің (ROS) пайда болуына байланысты.
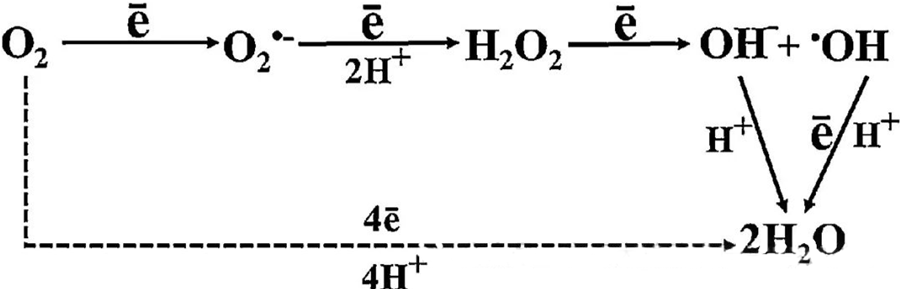
O₂ мен жасушалық компоненттер арасындағы өзара әрекеттесу ROS жасушаларында қалай пайда болатынын түсіну үшін өте маңызды. Тотығу стрессі деп аталатын белгілі бір жағдайларда ROS түзілуі мен оның ыдырауы арасындағы тепе-теңдік бұзылады, бұл жасушаларда ROS деңгейінің жоғарылауына әкеледі. Супероксидтің (O₂⁻) өндірілуі супероксиддисмутазамен катализденеді, ол кейіннен O₂⁻ сутегі асқын тотығына (H₂O₂) айналады. Бұл түрлендіру Фентон реакциясымен одан әрі күшейеді, ол Fe²⁺ тотықтырып, гидроксил радикалдарын (·OH) және Fe³⁺ түзеді, осылайша ROS түзілуінің және жасушалық зақымданудың зиянды тотығу-тотықсыздану тізбегін бастайды.
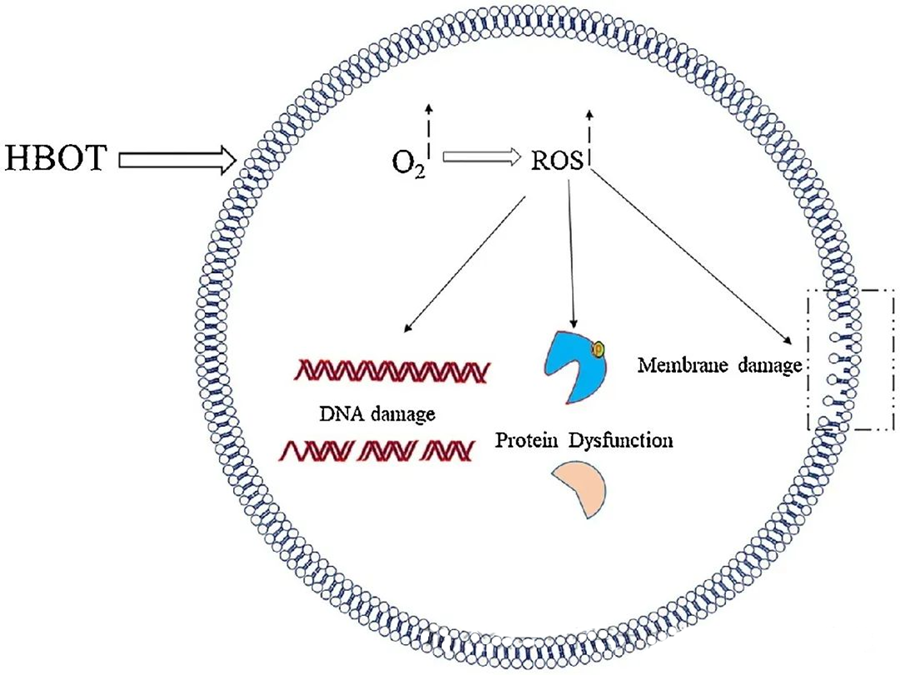
ROS-тың уытты әсері ДНҚ, РНҚ, ақуыздар және липидтер сияқты маңызды жасушалық компоненттерге бағытталған. Атап айтқанда, ДНҚ H₂O₂ арқылы цитоуыттылықтың негізгі нысанасы болып табылады, себебі ол дезоксирибоза құрылымдарын бұзады және негізгі құрамдарды зақымдайды. ROS тудыратын физикалық зақым ДНҚ-ның спираль құрылымына да таралады, бұл ROS тудыратын липидтердің асқын тотығуынан болуы мүмкін. Бұл биологиялық жүйелердегі ROS деңгейінің жоғарылауының жағымсыз салдарын көрсетеді.
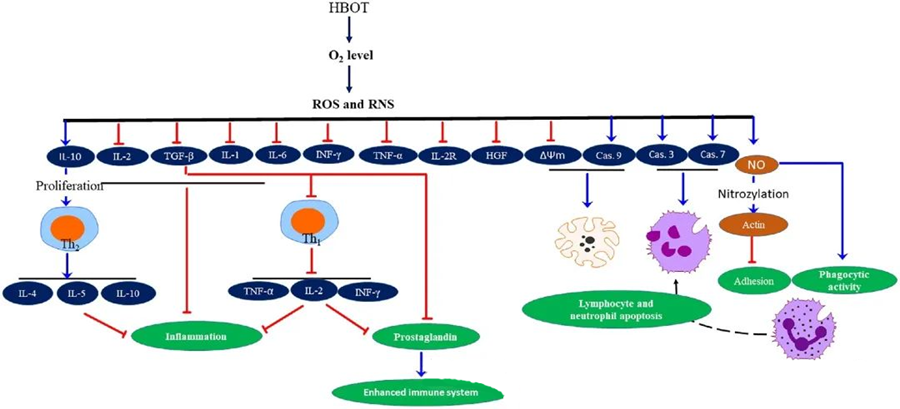
ROS микробқа қарсы әсері
HBOT индукцияланған ROS генерациясы арқылы көрсетілгендей, ROS микробтардың өсуін тежеуде маңызды рөл атқарады. ROS-тың уытты әсері ДНҚ, ақуыздар және липидтер сияқты жасушалық құрамдас бөліктерге тікелей әсер етеді. Белсенді оттегі түрлерінің жоғары концентрациясы липидтерді тікелей зақымдауы мүмкін, бұл липидтердің асқын тотығуына әкеледі. Бұл процесс жасуша мембраналарының тұтастығын және, демек, мембранамен байланысты рецепторлар мен ақуыздардың функционалдығын бұзады.
Сонымен қатар, ROS-тың маңызды молекулалық нысаналары болып табылатын ақуыздар цистеин, метионин, тирозин, фенилаланин және триптофан сияқты әртүрлі аминқышқылдарының қалдықтарында арнайы тотығу модификацияларына ұшырайды. Мысалы, HBOT E. coli-дегі бірнеше ақуыздарда, соның ішінде G элонгация факторы мен DnaK-да тотығу өзгерістерін тудыратыны, осылайша олардың жасушалық функцияларына әсер ететіні көрсетілген.
HBOT арқылы иммунитетті күшейту
HBOT қабынуға қарсы қасиеттеріқұжатталған, тіндердің зақымдануын жеңілдету және инфекцияның өршуін басу үшін маңызды екендігі дәлелденген. HBOT цитокиндер мен басқа қабыну реттегіштерінің экспрессиясына айтарлықтай әсер етеді, иммундық жауапқа әсер етеді. Әртүрлі эксперименттік жүйелер HBOT-тан кейін ген экспрессиясы мен ақуыз генерациясының әртүрлі өзгерістерін байқады, олар өсу факторлары мен цитокиндерді жоғарылатады немесе төмендетеді.
HBOT процесі кезінде O₂ деңгейінің жоғарылауы қабыну медиаторларының бөлінуін басу және лимфоциттер мен нейтрофилдердің апоптозын ынталандыру сияқты бірқатар жасушалық реакцияларды тудырады. Жалпы алғанда, бұл әрекеттер иммундық жүйенің микробқа қарсы механизмдерін күшейтеді, осылайша инфекциялардың жазылуын жеңілдетеді.
Сонымен қатар, зерттеулер HBOT кезінде O₂ деңгейінің жоғарылауы интерферон-гамма (IFN-γ), интерлейкин-1 (IL-1) және интерлейкин-6 (IL-6) сияқты қабынуға қарсы цитокиндердің экспрессиясын төмендетуі мүмкін екенін көрсетеді. Бұл өзгерістерге CD4:CD8 Т жасушаларының арақатынасын төмендету және басқа еритін рецепторларды модуляциялау, сайып келгенде, қабынуды болдырмау және жазылуды ынталандыру үшін маңызды болып табылатын интерлейкин-10 (IL-10) деңгейін көтеру де кіреді.
HBOT-тың микробқа қарсы белсенділігі күрделі биологиялық механизмдермен өзара байланысты. Супероксид те, жоғары қысым да HBOT тудыратын бактерияға қарсы белсенділікті және нейтрофилдердің апоптозын тұрақты түрде күшейтетіні туралы хабарланған. HBOT-тан кейін оттегі деңгейінің айтарлықтай жоғарылауы иммундық жауаптың маңызды компоненті болып табылатын нейтрофилдердің бактерицидтік қабілетін арттырады. Сонымен қатар, HBOT нейтрофилдердің адгезиясын басады, бұл нейтрофилдердегі β-интегриндердің эндотелий жасушаларындағы жасушааралық адгезия молекулаларымен (ICAM) өзара әрекеттесуі арқылы жүзеге асады. HBOT нейтрофилдердің β-2 интегринінің (Mac-1, CD11b/CD18) белсенділігін азот оксиді (NO) арқылы жүзеге асырылатын процесс арқылы тежейді, бұл нейтрофилдердің инфекция орнына миграциясына ықпал етеді.
Цитоскелеттің дәл қайта құрылуы нейтрофилдердің патогендерді тиімді фагоцитизациялауы үшін қажет. Актиннің S-нитрозилденуі актин полимерленуін ынталандыратыны, HBOT алдын ала емдеуден кейін нейтрофилдердің фагоцитарлық белсенділігін жеңілдететіні көрсетілген. Сонымен қатар, HBOT митохондриялық жолдар арқылы адам Т жасушаларында апоптозды ынталандырады, HBOT-тан кейін лимфоциттердің өлімінің жеделдетілгені туралы хабарланған. Каспаза-8-ге әсер етпей, каспаза-9-ды блоктау HBOT-тың иммуномодуляциялық әсерін көрсетті.
HBOT-тың микробқа қарсы агенттермен синергетикалық әсері
Клиникалық қолданыстарда HBOT инфекциялармен тиімді күресу үшін антибиотиктермен бірге жиі қолданылады. HBOT кезінде қол жеткізілетін гипероксидті күй белгілі бір антибиотикалық агенттердің тиімділігіне әсер етуі мүмкін. Зерттеулер β-лактамдар, фторхинолондар және аминогликозидтер сияқты нақты бактерицидтік препараттар тек ішкі механизмдер арқылы ғана емес, сонымен қатар бактериялардың аэробты метаболизміне ішінара тәуелді екенін көрсетеді. Сондықтан, оттегінің болуы және патогендердің метаболикалық сипаттамалары антибиотиктердің емдік әсерін бағалау кезінде маңызды рөл атқарады.
Оттегінің төмен деңгейі Pseudomonas aeruginosa-ның пиперациллин/тазобактамға төзімділігін арттыра алатынын және оттегінің төмен ортасы Enterobacter cloacae-нің азитромицинге төзімділігінің артуына ықпал ететінін дәлелдейтін маңызды дәлелдер бар. Керісінше, белгілі бір гипоксиялық жағдайлар бактериялардың тетрациклин антибиотиктеріне сезімталдығын арттыруы мүмкін. HBOT аэробты метаболизмді индукциялау және гипоксиялық жұқтырған тіндерді қайта оттегімен қанықтыру арқылы өміршең қосымша терапиялық әдіс ретінде қызмет етеді, кейіннен патогендердің антибиотиктерге сезімталдығын арттырады.
Клиникаға дейінгі зерттеулерде HBOT-ты (тәулігіне екі рет 280 кПа қысыммен 8 сағат бойы) тобрамицинмен (тәулігіне 20 мг/кг) бірге қолдану Staphylococcus aureus жұқпалы эндокардитінде бактериялық жүктемені айтарлықтай төмендетті. Бұл HBOT-тың қосымша емдеу әдісі ретіндегі әлеуетін көрсетеді. Әрі қарай жүргізілген зерттеулер 37°C температурада және 3 ATA қысымында 5 сағат бойы HBOT имипенемнің макрофагтармен жұқтырылған Pseudomonas aeruginosa-ға қарсы әсерін айтарлықтай күшейткенін көрсетті. Сонымен қатар, HBOT-ты цефазолинмен біріктірілген қолдану жануарлар модельдерінде Staphylococcus aureus остеомиелитін емдеуде цефазолинмен салыстырғанда тиімдірек екені анықталды.
HBOT сонымен қатар ципрофлоксациннің Pseudomonas aeruginosa биоүлбірлеріне қарсы бактерицидтік әсерін айтарлықтай арттырады, әсіресе 90 минуттық әсер етуден кейін. Бұл күшею эндогендік реактивті оттегі түрлерінің (ROS) түзілуіне байланысты және пероксидаза ақауы бар мутанттарда жоғары сезімталдықты көрсетеді.
Метициллинге төзімді Staphylococcus aureus (MRSA) тудырған плеврит модельдерінде ванкомициннің, тейкопланиннің және линезолидтің HBOT-пен бірлескен әсері MRSA-ға қарсы тиімділігінің айтарлықтай артқанын көрсетті. Диабеттік табан инфекциялары (DFI) және хирургиялық орн инфекциялары (SSI) сияқты ауыр анаэробты және полимикробты инфекцияларды емдеуде кеңінен қолданылатын антибиотик метронидазол анаэробты жағдайларда жоғары микробқа қарсы тиімділік көрсетті. HBOT-тың метронидазолмен бірге in vivo және in vitro жағдайларында синергетикалық бактерияға қарсы әсерлерін зерттеу үшін болашақ зерттеулер қажет.
HBOT-тың төзімді бактерияларға қарсы микробқа қарсы тиімділігі
Төзімді штамдардың эволюциясы мен таралуымен дәстүрлі антибиотиктер уақыт өте келе өз күшін жоғалтады. Сонымен қатар, HBOT көп дәріге төзімді патогендер тудыратын инфекцияларды емдеуде және алдын алуда маңызды болуы мүмкін, антибиотикалық емдеу сәтсіз болған кезде маңызды стратегия ретінде қызмет етеді. Көптеген зерттеулер HBOT-тың клиникалық тұрғыдан маңызды төзімді бактерияларға айтарлықтай бактерицидтік әсері туралы хабарлады. Мысалы, 2 ATM-де 90 минуттық HBOT сеансы MRSA өсуін айтарлықтай төмендетті. Сонымен қатар, қатынас модельдерінде HBOT әртүрлі антибиотиктердің MRSA инфекцияларына қарсы бактерияға қарсы әсерін күшейтті. Есептер HBOT-тың OXA-48 өндіретін Klebsiella pneumoniae тудырған остеомиелитті емдеуде ешқандай қосымша антибиотиктерді қажет етпей тиімді екенін растады.
Қорытындылай келе, гипербариялық оттегі терапиясы инфекцияны бақылаудың көп қырлы тәсілін білдіреді, иммундық жауапты күшейтеді, сонымен қатар қолданыстағы микробқа қарсы агенттердің тиімділігін арттырады. Кешенді зерттеулер мен әзірлемелердің арқасында ол антибиотиктерге төзімділіктің әсерін азайтуға мүмкіндік береді, бұл бактериялық инфекцияларға қарсы күресте үміт береді.
Жарияланған уақыты: 2025 жылғы 28 ақпан

